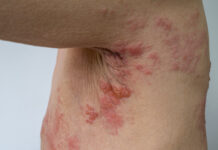
I augusti förra året godkändes läkemedlen Yescarta (axikabtagenciloceucel) och Kymriah (tisagenlekleucel) på den europeiska marknaden. Båda är immunterapier, så kallade CAR-T-terapier och godkända för behandling av blodcancerformerna storcelligt B-cellslymfom respektive akut lymfatisk leukemi, där de bedöms ha stor potential.
I ett utlåtande från NT-rådet rekommenderas dock regionerna att avvakta med att ge CAR-T-behandling. NT-rådets bedömning av läkemedlen är inte klar än.
– CAR-T-terapi innebär en viktig behandlingsmöjlighet vid mycket svåra sjukdomar. Det är väldigt angeläget att den här frågan hanteras så fort som möjligt. Om behandlingarna ska införas är det viktig att sker på ett rättvist och jämlikt sätt över Sverige och vi behöver värdera nytta i förhållande till kostnader så att behandlingarna verkligen kan komma rätt patienter till del, säger Gerd Lärfars, ordförande i NT-rådet.
Vid CART-T-terapi tas vita blodkroppar (T-celler) ut från patienten och modifieras genetiskt så att de kan känna igen och döda en viss typ av cancerceller. De modifierade cellerna förs tillbaka till patienten och bekämpar cancersjukdomen.
De kliniker som ska genomföra behandlingarna måste ackrediteras av de läkemedelsbolag som marknadsför CAR-T-läkemedlen, vilket enligt NT-rådet kräver både praktiskt och juridiskt arbete.
NT-rådet anger också att man arbetar med att ta fram en ”sammanvägd bedömning av behandlingarnas värde utifrån den etiska prioriteringsplattformen”. Tills bedömningen är klar avråder man alltså regionerna från att ge CAR-T-terapi. Bedömningen av läkemedlen väntas bli klar under våren, meddelar NT-rådet.
CAR-T bedöms har stor potential för behandling av vissa cancerformer, samtidigt som osäkerheten kring risk och nytta är stor, något som Läkemedelsvärlden rapporterat om. Prislappen är också hög och beräknas till cirka 3,5 miljoner kronor per behandling. Till skillnad från standardbehandling med cytostatika är dock CAR-T-terapi en engångsbehandling.