För första gången har ett läkemedel med gensaxen Crispr/Cas9 nu kommit så långt i utvecklingen att ansökningar om godkännande hamnat på läkemedelsmyndigheters bord. Det är företagen Vertex och Crispr Therapeutics som gemensamt ansökt om läkemedelsgodkännanden i USA, EU och Storbritannien.
Läkemedlet bär substansnamnet exagamglogene autotemcel som förkortas exa-cel. Det är en behandling av två ärftliga rubbningar av det syretransporterande proteinet hemoglobin i blodet. Närmare bestämt de allvarliga sjukdomarna sickelcellsanemi beta-thalassemi.
Fler läkemedel med gensaxen på gång
Genterapikandidaten exa-cel är baserat på genredigeringstekniken Crispr/Cas9. En teknik som år 2020 gav forskarna Emmanuelle Charpentier och Jennifer A. Doudna Nobelpriset i kemi.
Året dessförinnan tilldelade också Apotekarsocieteten Emmanuelle Charpentier Scheelepriset för den banbrytande upptäckten av gensaxen. Då menade experter att det återstod många år innan det skulle bli aktuellt att använda gensaxen för sjukdomsbehandling av patienter.
Men utvecklingen går nu i snabbt tempo. Företag och akademiska forskare utvecklar läkemedel med gensaxen mot en rad genetiska sjukdomar. Flera läkemedelskandidater har också redan nått klinisk fas där patienter får behandlingen.
”Häpnadsväckande utveckling”
I en artikel i tidningen Nature kommenterar en av gensaxens två upptäckare, Jennifer Doudna, de första läkemedelsansökningarna:
– Det är häpnadsväckande, säger hon, och jämför med vad man tänkte och trodde vid tiden för crispr-upptäckten för ett decennium sedan.
– Det var uppenbart att möjligheten att redigera arvsmassan var ett kraftfullt verktyg, men jag tror ingen av oss kunde föreställa sig hur snabbt forskningsfältet skulle röra sig.
Jennifer Doudna är själv medgrundare av två företag som utvecklar genredigerande läkemedel, Editas och Intellia. Det senare arbetar bland annat med gensaxbaserad genterapi mot den sällsynta Skelleftesjukan.
Emmanuelle Charpentier är å sin sida medgrundare av Crispr therapeutics, ett av de två företagen bakom den nu aktuella ansökan om godkännande av exa-cel.
Kan ge svåra komplikationer
Sickelcellsanemi och beta-thalassemi beror på mutationer i de gener som styr tillverkningen av hemoglobin. Vid beta-thalassemi leder bristen på normalt hemoglobin till anemi, brist på röda blodkroppar.
Anemin gör att olika delar av kroppen får för lite syre. Barn med svåra former av sjukdomen växer långsammare, utvecklingen kan bli fördröjd och skelettet skört. Sjukdomen kan även leda till hjärtsvikt.
Behandlingen består bland annat av regelbundna blodtransfusioner.
Svåra smärtor vid sickelcellanemi
Vid sickelcellsanemi får de röda blodkropparna en förändrad, halvmåneliknande form och kortare livslängd. Blodet blir mer trögflytande och skadade röda blodkroppar fastnar lätt på blodkärlens väggar.
Det försämrar blodcirkulationen och blodkärl kan bli igentäppta. Det uppstår därför syrebrist i kroppens vävnader vilket kan orsaka akut smärta.
Sickelcellsanemi kan ge allvarliga komplikationer som infektioner, bensår, njurskador och proppar och blödningar i hjärnan. Dagens läkemedelsbehandling inriktas på att lindra smärta och andra symtom. Hos vissa patienter kan sjukdomen också botas med hjälp av stamcellstransplantation.
Läkemedel med gensaxen häver blodbrist
Med det nya gensaxläkemedlet exa-cel siktar företagen på att varaktigt höja nivån av fungerande hemoglobin vid såväl beta-thalassemi som sickelcellsanemi. Därigenom ska man kunna häva blodbristen och dess svåra följdverkningar.
Behandlingsproceduren är dock komplicerad. Blodbildande stamceller från patientens benmärg tas i ett första steg ut och förändras sedan utanför kroppen med hjälp av exa-cel. Sedan får patienten tillbaka de förändrade stamcellerna genom en benmärgstransplantation.
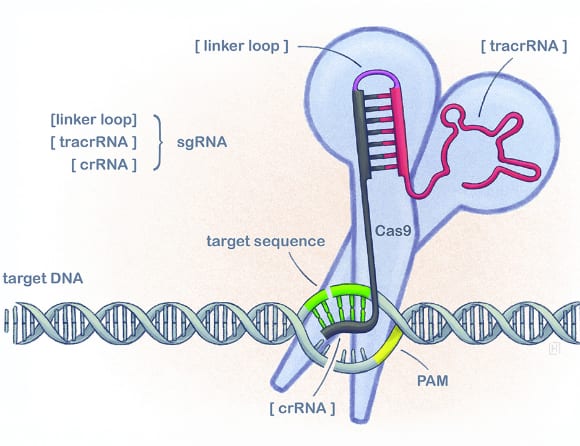
I exa-cel används gensaxens precisa förmåga att klippa DNA (se faktaruta) till att tysta en gen. Det är en gen som håller nere produktionen av så kallat fetalt hemoglobin.
Utvärderas i öppen studie
Sådant fetalt hemoglobin produceras normalt bara hos fostret och det lilla spädbarnet. Några månader efter födelsen inaktiveras produktionen av den gen som är i fokus för behandlingen med exa-cel. Genom att tysta denna gen hos de skördade stamcellerna och sedan återföra dem till patienten får man i gång produktionen av fetalt hemoglobin igen.
Detta har visat sig kunna höja patienternas hemoglobinnivåer och ge goda behandlingseffekter. Exa-cel utvärderas löpande under 15 år i två pågående öppna fas I-III-studier.
Resultat som företagen rapporterat visar bland annat att 42 av 44 patienter med beta-thalassemi klarade sig utan blodtransfusioner under en uppföljningstid på i genomsnitt ett drygt år.
Säkerheten en nyckelfråga
Hos de 31 exa-cel-behandlade patienterna med sickelcellsanemi förekom inga episoder med igentäppta kärl under i genomsnitt närmare tio månader. Före behandlingen hade de i genomsnitt fyra sådana allvarliga episoder om året.
Under ett par månader efter behandlingen är dock patienten mycket infektionskänslig. Några fall av allvarliga biverkningar av benmärgsbehandlingen har också förekommit, bland annat för lågt antal blodplättar, trombocytepeni.
Det finns också farhågor att genredigeringen ska kunna få oönskade genetiska bieffekter, men säkerhetsövervakningen i studien har ännu inte visat på några sådana.
Vilka kommer att ha råd?
En annan omdiskuterad fråga är vad detta läkemedel med gensaxen kan komma att kosta om det i framtiden blir godkänt. Inte minst mot bakgrund av att sickelcellsanemi och beta-thalassemi är särskilt vanliga i många fattiga länder i bland annat Afrika. Hur många av dem som skulle ha nytta av genterapin kommer verkligen att kunna få tillgång till den?
Det tongivande hälsoekonomiska analysorganisationen Icer (Institute for clinical and economic review) presenterade nyligen en tidig bedömning av exa-cel. Enligt denna kan behandlingen vara kostnadseffektiv vid en prisnivå på upp till 1,7 miljoner US-dollar för en patient, omkring 17,5 miljoner svenska kronor.
Denna prognos ger möjligen en fingervisning om var ett framtida pris på exa-cel skulle kunna hamna.