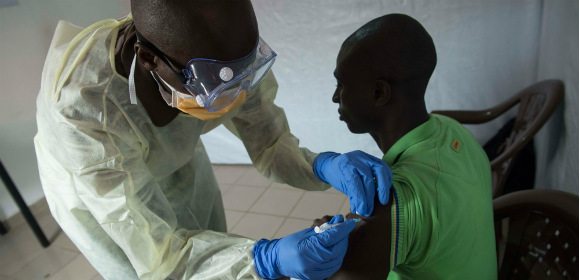
Vaccinkandidaten V920 testades i en fas III-prövning under det pågående ebolautbrottet i Västafrika 2015, något som Läkemedelsvärlden.se skrivit om tidigare. Effekten visade sig vara god och de som fick vaccinet utvecklade antikroppar mot ebolaviruset och ingen av de vaccinerade fick sjukdomen.
I den aktuella studien var uppföljningstiden 84 dagar och frågetecken kvarstod om hur varaktigt skydd vaccinet gav.
I en nu publicerad studie i The Lancet Infectius Diseases visar ett internationellt forskarlag att vaccinet tycks ge ett skydd som består i minst två år efter vaccinationstillfället – sannolikt längre.
Den observationella kohort-studien innebar att forskarna poolade data från friska frivilliga som fått vaccinet, som utvecklats av bland annat läkemedelsbolaget MSD, i tre olika fas I-studier. En studie utfördes i Genéve i Schweiz, en i Labaréné i Gabon och en i Kilifi i Kenya. Totalt ingick 217 personer i de tre studierna.
Det primära effektmåttet var immunsvar mätt som glykoproteinspecifik IgG-koncentration och mättes ett respektive två år efter vaccination.
I ettårsuppföljningen medverkade försökspersoner från alla studierna, 197 av 217 personer, medan tvåårsuppföljningen enbart innehöll personer från Genéve-studien, totalt 90 personer.
Forskarna konstaterade att studiedeltagarna hade höga och stabila koncentrationer av antikroppar mot ebolaviruset, såväl ett år som två år efter vaccinering. I studierna gavs vaccinet i två olika doser, antingen i en hög dos eller i en lägre. Den högre dosen gav ett starkare immunsvar men även den lägre innebar att personerna utvecklade stabila nivåer av antikroppar i tillräckligt hög grad.
Resultaten visar att vaccinet ger ett skydd i åtminstone två år och att det räcker med en dos vaccin för att uppnå skyddet. Det har stor betydelse för möjligheten att kontrollera smittan i sjukdomsdrabbade områden liksom för att ge hjälparbetare ett skydd inför insatser på plats.
– Det här är verkligen goda nyheter eftersom detta vaccin är avsett för platser där det ofta är väldigt svårt med logistiken. Att behöva ge en booster-dos i dessa områden skulle vara mycket opraktiskt, säger Angela Huttner, specialist i infektionssjukdomar vid universitetssjukhuset i Genéve och huvudförfattare till studien, till nyhetssajten STAT News.
Vaccinet finns ännu inte på marknaden, men enligt MSD är målet att lämna in en ansökan om marknadsgodkännande till den amerikanska läkemedelsmyndigheten FDA under 2018.
Studien finansierades av Wellcome Trust och Innovative medicines initiative, IMI.